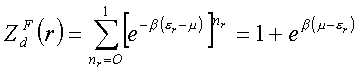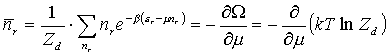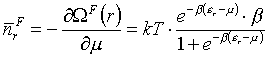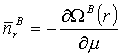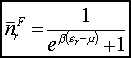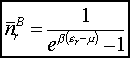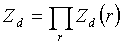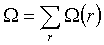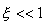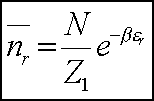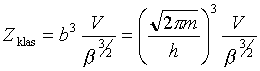idż do fizyka kwantowa. 2. Definicja i własności temperatury bezwzględnej; temperatura układów w równowadze cieplnej; pomiar temperatury. 3. Entropia (definicja mikroskopowa, małe przekazy ciepła); stan równowagi. 4. Układ kontaktujący się termicznie ze zbiornikiem ciepła (rozkład kanoniczny). 5. Paramagnetyzm (prawo Curie). Ciepło właściwe oscylatora harmonicznego. 6. Średnia energia i średnie ciśnienie gazu doskonałego. 7. Twierdzenie o wiriale w zastosowaniu do gazu doskonałego. Gazy rzeczywiste. 8. Ogólne równanie stanu gazów doskonałych. 9. Twierdzenie o ekwipartycji energii (wyprowadzenie i przykłady). 10. Maxwellowski rozkład prędkości. 11. Entropia gazu doskonałego; równanie adiabaty. 12. Zasady termodynamiki i związki statystyczne. Sprawność silnika. Cykl Carnota. 13. Potencjały termodynamiczne (wyprowadzenia) i tożsamości Maxwella. 14. Prawo Steana-Boltzmana. Prawo Wina. 15. Stan równowagi pomiędzy fazami; równanie Clausiusa - Clapeyrona. 16. Układy otwarte. Statystyki kwantowe. Granica klasyczna. 17. Rozkład Plancka. 18. Gęstość stanów w przestrzeniach 1, 2, 3-wymiarowych. Periodyczne a sztywne warunki brzegowe. 19. Gaz elektronów swobodnych. 20. Półprzewodniki: gęstość nośników, prawo działania mas, potencjał chemiczny. |
Opracowali: J. Ropka, B. Wróbel. Konsultacje: J. Wolny 16. Układy otwarte. Statystyki kwantowe. Granica klasyczna.
Duży zespół kanoniczny.Zespół kanoniczny Duże otoczenie z określoną liczbą cząstek utrzymuje temperaturę; stała objętość, potencjał chemiczny. Zmiana ciepła i zmiana liczby cząstek nie zaburza otoczenia. E0 - całkowita energia-stała N0 - całkowita liczba cząstek-stała S0- entropia otoczenia
Duża funkcja rozdziału:
Statystyki kwantoweZałóżmy, że cząstki gazu doskonałego są nierozróżnialne, nie możemy śledzić indywidualnej cząstki. Wybieramy jakiś poziom energetyczny i obserwujemy jego obsadzenie - podukład. Jest to układ otwarty.W gazie doskonałym
Wtedy dla podukładu- dla konkretnego poziomu energetycznego
Mamy dwa rodzaje cząsteczek:
Średnia liczba cząsteczek:
Dla całego układu:
Granice klasyczneDla małych nr pomijamy jedynkę w mianowniku
Statystyka klasyczna dobrze działa dla małego parametru zwyrodnienia. Dla dużej wartości parametru zwyrodnienia musimy używać statystyki kwantowej.
Przykłady:
Zatem hel gazowy można traktować jak gaz doskonały. góra |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
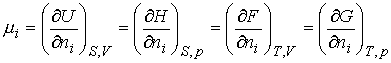
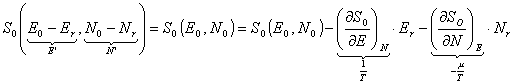
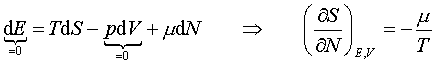
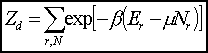
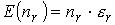
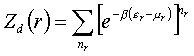
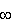 np. fotony.
np. fotony.